지엔티파마가 올해 하반기 치매약 '크리스데살라진' 임상 2상에 대한 식약처 승인을 추진한다.
반려견 치매 3상 종료에 따라 인간을 대상으로 한 임상에도 자신감이 붙었기 때문이다.
14일 지엔티파마는 반려견 치매(인지기능저하 증후군) 치료제로 개발 중인 약물 크리스데살라진의 임상 3상 시험을 성공적으로 완료했다고 14일 발표했다.
중증 인지기능장애를 겪고 있는 48마리의 반려견을 대상으로 1년에 걸쳐 진행한 임상연구에서 크리스데살라진 투여군은 일차 유효성 평가지표인 반려견 '인지기능장애 지수'와 이차 유효성 평가지표인 '반려견 치매 지수'에서 플라시보 대조군에 비해 유의적인 약효가 입증됐다.
탁월한 인지기능개선 약효는 5mg/kg 또는 10mg/kg 크리스데살라진을 투여한 반려견에서 투약개시 4주와 8주에 모두 유의적으로 나타났다. 크리스데살라진의 투약과 관련한 부작용은 발견되지 않았다.
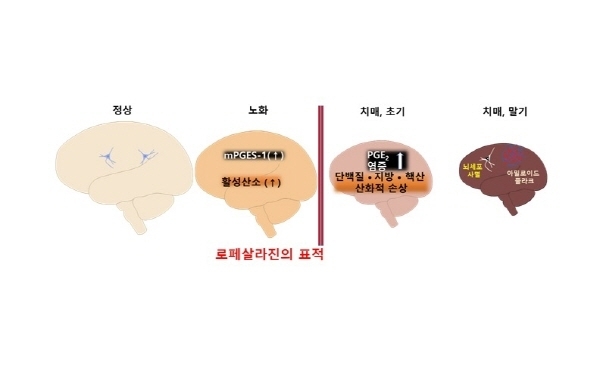
크리스데살라진은 과학기술부와 보건복지부의 지원을 받아 개발된 치매 치료 신약물질로, 알츠하이머 치매와 반려견 치매를 유발하는 아밀로이드 플라크, 타우 단백질 침착, 뇌신경세포 사멸을 막기 위해 강력한 항산화 작용과 안전한 소염 작용을 동시에 보유하도록 발굴된 다중표적 약물이다.
지엔티파마 연구진은 크리스데살라진이 치매 쥐 모델에서 아밀로이드 플라크와 뇌신경세포의 사멸을 줄이고 인지기능을 개선하는 효과를 입증한 바 있다.
크리스데살라진의 임상 3상 연구에는 서울대학교 동물병원 내과, 대구 동물메디컬 센터, 부산 제일2차 동물메디컬센터, 해마루 동물병원, 헬릭스 동물메디컬센터, N동물의료센터, VIP 동물의료센터에서 참여했고, 중증 치매를 앓고 있는 총 48마리의 반려견을 대상으로 진행했다.
지엔티파마의 동물 헬스케어 사업부 대표인 이진환 박사는 “반려견 치매에서 크리스데살라진의 안전성은 물론 탁월한 약효가 입증된 것은 획기적인 결과”라며 “신속하게 연구결과 보고서를 마무리해서 농림축산검역본부에 2월중으로 신약승인을 신청할 예정”이라고 말했다.
회사 측은 "크리스데살라진의 약효가 사람 알츠하이머 치매와 증상과 병인이 유사한 반려견 치매 임상 3상연구에서 입증됨에 따라, 알츠하이머 치매 치료제 개발에 대한 기대감이 크다"고 설명했다.
지엔티파마 대표이자 개발자인 곽병주 박사는 “중증 치매견에서 투여한지 4주 만에 크리스데살라진의 약효가 확연히 나타났기 때문에, 알츠하이머 치매 환자에 대한 임상 2상 연구는 2-3년이면 완료할 수 있을 것”이라며, “올 하반기에는 식약처에 크리스데살라진의 알츠하이머 치매 임상연구를 신청할 계획”이라고 덧붙였다.


